Sujet : Essais cliniques / Découvertes médicales
Le nouvel inhibiteur de SGLT2 de Daewoong Pharmaceutical, destiné au traitement du diabète, produit des résultats remarquables lors d'un essai clinique de phase 2
- Daewoong a annoncé le résultat de l'essai clinique de phase 2 de l'Enavogliflozin à l'occasion de l'ICDM 2020.
- la société veut accélérer la recherche et le développement pour agrandir sa présence sur le marché mondial en établissant des partenariats complets à l'étranger
SÉOUL, Corée du Sud, 29 septembre 2020 /PRNewswire/ -- Daewoong Pharmaceutical (Daewoong) (PDG : Sengho Jeon) a annoncé pour la première fois le résultat de son essai de phase 2 sur l'enavogliflozin, un nouvel inhibiteur de SGLT2, lors du Congrès international du diabète et du métabolisme (ICDM), qui s'est tenu les 18 et 19 septembre.
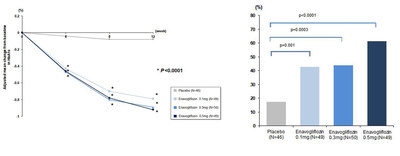
Les patients du diabète de type 2 ayant pris de l'enavogliflozin en monothérapie pendant 12 semaines ont constaté à partir de la semaine 4 des réductions statistiquement significatives de leur taux d'hémoglobine glyquée (HbA1c), par rapport aux traitements à base de placébo. À la semaine 12, le taux d'HbA1c des patients a diminué d'environ 0,9%p de plus par rapport au placébo. Il s'agit d'un résultat statistiquement significatif qui indique que l'enavogliflozin a entraîné une réduction du taux d'HbA1c environ 0,2 à 0,3 %p supérieure que celle des autres inhibiteurs de SGLT2, pour lesquels des essais ont été menés dans des pays occidentaux. Ce résultat élève donc les attentes par rapport aux études futures.
Jusqu'à 61 % des patients avaient un taux d'HbA1c supérieur à 7,0%* à la semaine 12, soit une augmentation de plus de 20%p par rapport aux patients qui ont participé aux essais des inhibiteurs existants du SGLT2. De plus, 72 % des patients ont vu leur taux d'HbA1c baisser de plus de 0,5 % au cours de la semaine 12, ce qui montre que la glycémie a diminué de façon notable chez les patients, y compris chez ceux qui n'ont pas répondu aux autres inhibiteurs de SGLT2.
Il convient également de noter que seulement 2 % des patients ont contracté une infection génitale ou une infection des voies urinaires, deux effets secondaires du mécanisme des inhibiteurs de SGLT2. Cela confirme l'innocuité exceptionnelle du médicament. Ce taux est nettement inférieur à celui des inhibiteurs de SGLT2 développés par d'autres sociétés, qui varie entre 5 et 10 %.
Le Dr Kyongsoo Park, chercheur et coordonnateur de l'essai, a déclaré : « Le résultat de l'essai de phase 2 de l'enavogliflozin, durant lequel le médicament a été administré en monothérapie à 200 patients coréens, confirme son excellente capacité à réduire la glycémie et son innocuité. Si cette efficacité et cette innocuité remarquables se confirment lors de la phase 3, dans le cadre d'un traitement en monothérapie ou en thérapie combinée, l'enavogliflozin devrait devenir un bon choix de traitement pour les patients atteintes du diabète de type 2. »
Sengho Jeon, PDG de Daewoong, a affirmé : « Au vu du résultat excellent produit par l'enavogliflozin, nous allons consacrer encore plus d'efforts pour mettre au point le meilleur inhibiteur de SGLT2 qui soit. Nous accélérerons la recherche et le développement pour agrandir notre présence sur le marché mondial en établissant des partenariats complets à l'étranger. »
Daewoong projette de lancer des essais cliniques de phase 3 liés à de multiples indications diabétiques cette année. L'entreprise s'est fixé l'objectif de commercialiser le médicament en Corée d'ici 2023. De plus, les indications de l'énavogliflozine devraient s'élargir pour inclure l'obésité, les maladies cardiaques et les maladies rénales, en plus du diabète.
Photo - https://mma.prnewswire.com/media/1283018/EU_enavogliflozin_phase_2_clinical_trial.jpg
Ces communiqués peuvent vous intéresser aussi
|
Communiqué envoyé le et diffusé par :