Sujets : Annonce - Ressources humaines, Essais cliniques / Découvertes médicales
iSTAR Medical reçoit l'approbation de la FDA des États-Unis pour démarrer l'essai pivot concernant MINIject chez les patients atteints de glaucome
Des chirurgiens de renommée mondiale se joindront à l'étude STAR-V d'iSTAR Medical
WAVRE, Belgique, 15 juillet 2021 /PRNewswire/ -- iSTAR Medical, une société de technologie médicale développant des micro-implants de drainage du glaucome (MIGS), a annoncé aujourd'hui que la Food and Drug Administration (FDA) des États-Unis lui a accordé une exemption des dispositifs expérimentaux (IDE) pour commencer un essai pivot avec MINIjectTM. L'étude STAR-V étudiera MINIjectTM chez plus de 350 patients atteints de glaucome primitif à angle ouvert. Des chirurgiens du glaucome de renommée mondiale aux États-Unis, au Canada et en Europe se joindront à l'essai.

L'essai STAR-V évalue l'efficacité de MINIjectTM par la réduction moyenne de la pression oculaire, ainsi que la proportion de patients obtenant une réduction d'au moins 20 % de la pression oculaire. Cette étude évaluera la sécurité et l'efficacité du MINIjectTM seul, dans une procédure non associée à une chirurgie simultanée de la cataracte. Les principaux résultats de l'étude seront disponibles lorsque tous les patients auront complété leur suivi à 2 ans dans l'étude. Les patients seront également suivis pour évaluer les bénéfices à long terme et la tolérance du MINIjectTM dans le traitement du glaucome léger à modéré.
Le Dr Brian E. Flowers, spécialiste du glaucome chez Ophthalmology Associates de Fort Worth, Texas, États-Unis, a déclaré : « Au nom des investigateurs, j'aimerais partager notre enthousiasme à l'idée de commencer l'essai STAR-V. L'espace supraciliaire de l'oeil est une voie d'écoulement naturelle qui s'est révélée très prometteuse. Il est possible d'améliorer l'efficacité de réduire la pression oculaire chez nos patients d'une manière moins invasive. L'accès à un dispositif efficace pour réduire la pression et utilisé dans une procédure autonome nous permettra d'offrir un traitement à beaucoup plus de patients atteints de glaucome avec une option de traitement mini-invasive. »
Michel Vanbrabant, PDG d'iSTAR Medical, a déclaré : « Nous sommes très heureux que la FDA nous ait accordé l'approbation afin d'apporter cette technologie innovante aux patients nord-américains souffrant de glaucome primitif à angle ouvert dans le cadre de l'essai STAR-V. Les résultats d'essais cliniques menés sur plus de 130 patients en Europe, en Asie et en Amérique latine ont démontré de manière constante que MINIjectTM conserve un profil de sécurité positif et offre une réduction significative de la pression grâce à notre matériau exclusif STAR et à la puissance de l'espace supraciliaire. »
À propos de iSTAR Medical
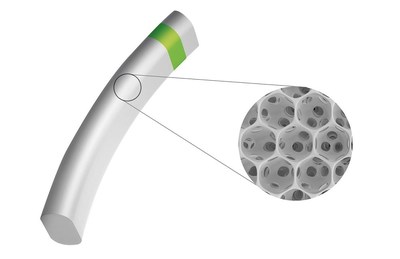
iSTAR Medical SA est une société privée de technologie médicale développant des implants ophtalmiques peu invasifs pour le traitement de patients atteints de glaucome. iSTAR Medical détient les droits exclusifs pour l'utilisation ophtalmique du matériau STAR®, développé par l'Université de Washington, à Seattle (États-Unis). STAR possède des propriétés antifibrotiques et anti-inflammatoires exceptionnelles, ainsi qu'une structure poreuse unique qui améliore l'écoulement du liquide naturel. iSTAR Medical a été fondée en 2011 et son siège social est situé à Wavre, en Belgique. www.istarmed.com
À propos de MINIjectTM
MINIject est le dispositif MIGS révolutionnaire d'iSTAR Medical destiné aux patients atteints de glaucome primitif à angle ouvert. MINIject allie la structure poreuse unique de son matériau STAR exclusif à la puissance offerte par l'espace supraciliaire. De ce fait, il est conçu pour améliorer l'écoulement du liquide naturel, réduire la pression intraoculaire (PIO) et le besoin de médicaments, tout en bio-intégrant les tissus environnants et en limitant l'inflammation, la fibrose et les complications ultérieures.
À propos du glaucome
Le glaucome est une maladie évolutive et la deuxième cause principale de cécité chez l'adulte,[1] touchant plus de 100 millions de personnes dans le monde.[2] La réduction de la PIO, au moyen de médicaments ou d'une intervention chirurgicale, permet de retarder la progression de la maladie.[1] Les médicaments sont généralement le traitement de première intention, mais l'ajout progressif de plusieurs gouttes peut supposer des effets secondaires pour les patients, des enjeux concernant l'observance et des coûts.[1,2] La chirurgie invasive peut présenter des risques de complications irréversibles.[1,2] Le MIGS est le traitement du glaucome le plus prometteur et à la croissance la plus rapide en raison de son profil d'innocuité amélioré.[2] MINIject est potentiellement le meilleur de sa catégorie pour son efficacité et sa sécurité d'emploi prometteuses à long terme.
[1] Terminologie et lignes directrices de l'European Glaucoma Society pour le glaucome, 4e édition : British Journal of Ophthalmology. 2017;101:1-195 https://bjo.bmj.com/content/101/5/73
[2] Glaucoma Surgical Device Market Report, publié par Market Scope, août 2020. https://www.market-scope.com/pages/reports/202/2020-glaucoma-surgical-device-market-report-a-global-analysis-for-2019-to-2025-august-2020
Photo - https://mma.prnewswire.com/media/1573698/MINIject_image_web.jpg
Logo - https://mma.prnewswire.com/media/1573697/iSTAR_Med_Logo.jpg
Ces communiqués peuvent vous intéresser aussi
|
Communiqué envoyé le et diffusé par :



