Sujets : Nouveaux produits et services, Essais cliniques / Découvertes médicales, Approbation de la FDA (Food and Drug Administration)
Triastek reçoit l'autorisation DNR de la FDA pour un médicament imprimé en 3D destiné au traitement de la colite ulcéreuse
- Troisième autorisation DNR de la FDA pour un médicament imprimé en 3D pour Triastek
- T21, un nouveau traitement potentiel capable d'administrer un médicament ciblant le côlon
NANJING, Chine, le 21 nov. 2022 /CNW/ -- Triastek, Inc. (« Triastek »), une entreprise mondiale du secteur de la santé, pionnière de l'impression 3D de produits pharmaceutiques grâce à sa technologie exclusive, Melt Extrusion Deposition (MED®), a annoncé aujourd'hui qu'elle avait reçu l'autorisation de la Food and Drug Administration (FDA) des États-Unis pour sa demande de nouveau médicament de recherche (DNR) afin de lancer des études cliniques sur le médicament imprimé en 3D T21, un traitement potentiel de la colite ulcéreuse.
« Nous sommes ravis d'avoir reçu l'autorisation DNR de procéder à des essais cliniques de ce traitement potentiellement transformateur pour les patients, a déclaré la Dre Senping Cheng, fondatrice et chef de la direction de Triastek. Il est difficile de retarder la libération des médicaments et d'administrer des formes pharmaceutiques orales dans le côlon. Le T21 offre donc une nouvelle option prometteuse pour les patients en permettant l'administration de médicaments à un site en particulier et ayant un effet localisé, ce qui atténue les effets secondaires potentiels de l'exposition systémique. Nous sommes impatients de faire progresser ce traitement en clinique et nous sommes reconnaissants du soutien de la FDA. »
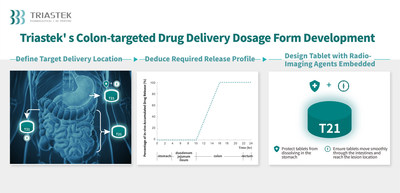
Le T21 est un nouveau traitement potentiel capable d'administrer un médicament ciblant le côlon. Grâce à une conception de forme pharmaceutique 3D unique, le T21 peut atteindre le segment du côlon ciblé dans le tractus gastro-intestinal, ce qui permet d'utiliser une dose de médicament inférieure à celle du médicament de référence, qui fournit une exposition systémique. Rendus possibles grâce à l'impression 3D, les agents d'imagerie radio intégrés à des composants particuliers de la forme pharmaceutique ont été utilisés au début du développement de la formulation afin d'évaluer et de confirmer le site de libération du médicament dans le tractus gastro-intestinal. Ce nouveau processus peut être utilisé dans le développement de futurs médicaments ciblant des segments précis du tractus gastro-intestinal afin d'accroître l'efficacité et le taux de succès du développement du produit. La plate-forme technologique de comprimés oraux à libération retardée et ciblant le côlon peut être utilisée non seulement pour le développement de médicaments à petites molécules, mais aussi de médicaments peptidiques.
Triastek avait déjà reçu l'autorisation DNR de la FDA pour ses produits T19 et T20 pour le traitement de la polyarthrite rhumatoïde et des troubles cardiovasculaires et de la coagulation, respectivement. Triastek continue de démontrer la large applicabilité de sa technologie MED® par l'avancement de produits qui résolvent un large éventail de problèmes d'administration de médicaments dans de multiples domaines thérapeutiques.
À propos de Triastek
Triastek, Inc. est une entreprise mondiale de soins de santé qui développe des médicaments grâce à une technologie d'impression 3D innovante et exclusive. Triastek est vouée à révolutionner le développement et la fabrication de produits pharmaceutiques et à libérer la prochaine génération de médicaments grâce à la technologie d'impression 3D. Sa technologie de pointe, appelée Melt-Extrusion Deposition (MED®), facilite le développement de médicaments construits en couches afin de permettre une libération contrôlée et précise des traitements. Cette conception de traitement optimisée aide à contrôler le moment, l'endroit et la quantité de médicaments libérés dans le corps, assurant une administration plus ciblée et efficace.
À propos de Melt-Extrusion Deposition (MED®)
L'impression 3D par Melt-Extrusion Deposition (MED®) est une technologie de fabrication additive de bout en bout qui convertit en continu des matières premières en poudre en états ramollis/fondus, suivis d'un dépôt précis couche par couche pour produire des objets aux structures géométriques bien conçues.
Photo - https://mma.prnewswire.com/media/1951682/image_5017147_11354335.jpg
Photo - https://mma.prnewswire.com/media/1951683/image_5017147_11354695.jpg
Logo - https://mma.prnewswire.com/media/1859327/global_Logo_Logo.jpg
SOURCE Triastek, Inc.
Ces communiqués peuvent vous intéresser aussi
|
Communiqué envoyé le et diffusé par :