Sujet : Essais cliniques / Découvertes médicales
Une équipe d'iHuman de l'université ShanghaiTech décrypte la structure du premier récepteur humain couplé aux protéines G de type Frizzled
SHANGHAI, 23 août 2018 /PRNewswire/ -- Le laboratoire Xu de l'institut iHuman de l'université ShanghaiTech a décrypté la structure cristalline à haute résolution du premier récepteur humain couplé aux protéines G de type Frizzled. En tant que protéine protégeant la régulation de la signalisation Wnt, qui joue un rôle fondamental dans le développement embryonnaire et la tumorigenèse, les récepteurs couplés aux protéines G de type Frizzled (FZD) ont été, sans succès, des cibles de médicaments anticancéreux pendant des décennies. Cependant, ces résultats qui illustrent l'architecture unique du récepteur Frizzled-4 dans son état sans ligand et expliquent la barrière éternelle qui empêche l'identification de ligands puissants pour cette famille de récepteurs favoriseront la recherche fondamentale et thérapeutique qui pourrait mener à la découverte de nouveaux médicaments essentiels. Ces nouvelles découvertes sont aujourd'hui publiées par Yang et al. dans l'édition en ligne avancée de la revue Nature, sous le titre Crystal structure of Frizzled 4 receptor in ligand-free state (Structure cristalline du récepteur Frizzled 4 à l'état sans ligand).
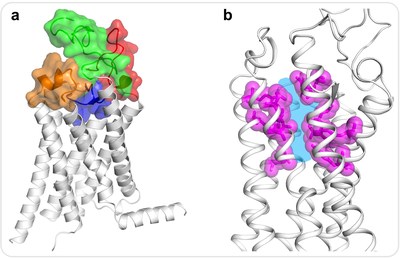
« Pour comprendre pourquoi personne n'a été capable de développer de bons ligands-outils ou des molécules médicamenteuses pour les FZD, nous avons déchiffré la structure intacte du domaine transmembranaire du récepteur Frizzled4 (FZD4) à une résolution de 0,24 nm (2,4 angströms) », a déclaré le professeur adjoint de l'institut iHuman et de l'École des sciences de la vie et de la technologie de l'université ShanghaiTech, et auteur correspondant de l'étude.
Les auteurs de l'étude ont été surpris de constater que le site de liaison du ligand orthostérique traditionnel est très étroit et hydrophile, ce qui rend difficile la pénétration ou la liaison de petites molécules. « Ces résultats nous aident à mieux comprendre le ligand et la signalisation FZD, et ils démontrent que la conception de ligands pour cette poche peut nécessiter des considérations particulières qui pourraient s'inspirer de cette structure cristalline », a ajouté Fei Xu.
« Pour créer une protéine humaine FZD4 plus stable, capable de déterminer la structure en l'absence de ligand, il a fallu quatre ans à l'équipe pour analyser des centaines de composants, optimiser les procédures de purification et tester des milliers de conditions de cristallisation conjecturales », a déclaré le chercheur boursier postdoctoral de l'institut iHuman et premier auteur de l'étude, Shifan Yang.
Outre la découverte d'une poche vide, l'étude fournit également un aperçu d'un mécanisme d'activation unique de la famille des récepteurs Frizzled. « Une structure aussi remarquable nous fournit un modèle plus précis pour réorienter les efforts sur la découverte de médicaments à base de récepteurs Frizzled », a déclaré le directeur de l'institut iHuman de l'Université ShanghaiTech, Raymond Stevens.
D'autres coauteurs de cet article proviennent de l'université ShanghaiTech, de l'institut de recherche Van Andel et de l'université de Californie du Sud.
Lien vers le texte complet l: http://dx.doi.org/10.1038/s41586-018-0447-x
Photo - https://mma.prnewswire.com/media/733364/Frizzled4.jpg
Ces communiqués peuvent vous intéresser aussi
|
Communiqué envoyé le et diffusé par :



